Не путать с фарад.
В Постоянная Фарадея
, обозначается символом
F
и иногда стилизованный под ℱ, назван в честь Майкл Фарадей. В химия и физика, эта константа представляет величину электрический заряд на крот из электроны.[1] Имеет текущее принятое значение
F
= 96485.33212… С · моль−1.[2]
Поскольку 1 моль электронов = 6.02214076×1023 электроны (Число Авогадро),[3] постоянная Фарадея равна элементарный заряд е
, величина заряда электрона, умноженная на 1 моль:[4]
F
= 96485.3… С / (1 моль) = 96485.3… С / (6.022 …×1023) = 1.60217663410×10−19 C =
е
Одним из распространенных способов использования постоянной Фарадея является электролиз расчеты. Сумму заряда можно разделить на кулоны постоянной Фарадея, чтобы найти химическое количество (в молях) элемента, который был окисленный.
Значение F
был впервые определен путем взвешивания количества серебро осажден в электрохимической реакции, в которой измеренный Текущий был пройден в течение отмеренного времени, и с помощью Закон электролиза Фарадея.[5]
Майкл Фарадей – основоположник закона индукции
Ученый занимавшиеся изучением электричества – великий английский физик и химик Майкл Фарадей (1791-1867). Его заслуга в изучении взаимной магнитной индукции между двумя связанными контурами как основа при производстве электричества огромна.
Будучи сыном кузнеца, он был самоучкой, благодаря книгам по химии и электричеству, которые он читал во время своего ученичества в переплетной мастерской—работу, которую он начал в возрасте 14 лет. Когда он был еще подростком, у него была возможность посещать лекции великого химика Хамфри Дэви в Королевском институте. В возрасте 21 года Дэви нанял его помощником в Королевский институт, где Фарадей оставался в течение следующих 50 лет, будучи назначен заведующим его лабораторией в 1821 году. Хотя отсутствие формального образования оставляло ему математические пробелы, они были в значительной степени компенсированы поразительной экспериментальной интуицией, которая позволила ему стать одним из самых влиятельных экспериментальных исследователей всех времен.
В 1821 году Фарадей начал исследовать взаимодействие между магнитами и токами. Он разработал концепцию силовой линии (термин, который он ввел) для обоснования фигур, образованных железными опилками вблизи магнита. Используя эту концепцию, в августе 1831 года он открыл взаимную магнитную индукцию, отметив переходный ток, индуцируемый в катушке, когда ток включался и выключался во второй катушке. Обе катушки были намотаны на один и тот же тороидальный железный сердечник.
В октябре 1831 года Фарадей наблюдал самоиндукцию, возникающую в результате тока, индуцируемого в соленоидальной катушке движением магнита внутри ее отверстия.
Фарадей ввел термин электродвижущая сила для такого эффекта, и мы все еще видим это в использовании сегодня.
В 1831 году Фарадей также создал представление электромеханического генератора. Он ввел понятие диэлектрической проницаемости и построил первый переменный конденсатор в 1837 году. Он также изучал оптику и поляризацию света вместе со своим другом Чарльзом Уитстоуном, открыв в 1845 году эффект Фарадея (вращение поляризованного света при прохождении через намагниченную область).
Между 1846 и 1855 годами Фарадей признал магнитные свойства материи и ввел понятие диамагнетизма. Развивая идею силовых линий, он ввел понятия электрического и магнитного полей.
Не менее важными были открытия Фарадея в области химии, где он написал несколько прорывных работ. Он собрал свою колоссальную научную продукцию главным образом в экспериментальных исследованиях, опубликованных в нескольких номерах между 1839 и 1855 годами. Он выступал с памятными лекциями в Королевском институте, был назначен членом Королевского общества в 1824 году и дважды получил медаль Копли, в 1832 и 1838 годах, но отказался от дворянского титула и президентства Королевского института (1864) и не хотел регистрировать никаких патентов.
Общие сведения
При пропускании электрического тока через раствор происходит физико-химический процесс, названный электролизом. Заключается он в способности выделения веществами вторичных продуктов. Термин произошёл от греческого λυσις, что в переводе обозначает «разрушение». Его понятие довольно точно описывает происходящий процесс.
Любое вещество состоит из совокупности связных атомов и молекул, которые образуют ионы при потере или присоединении электронов. Когда их количество превышает число протонов заряженная частица становится отрицательной. Называют её катионом. Если же ион потерял электрон, то он становится положительно заряженным. В этом случае его называют анионом.
Чтобы связи в веществе нарушились, тем самым электрически нейтральный ион получил знак, нужно выполнить какое-либо воздействие. Для жидкости это и есть электролиз — разделение частиц под действием электрического тока. Но при этом элементы обладают способностью диссоциировать. Другими словами, распадаться при смешивании на два или более молекулярных элемента. В 1887 году учёный Сванте Аррениус смог сформулировать теорию о диссоциации. Она в дальнейшем была дополнена положением о гидратации.
В результате ряда экспериментов все жидкие вещества были разделены на два вида:
- Электролиты — элементы проводящие электрический ток. К ним относятся вещества описывающиеся ковалентной полярной и ионной связью. Например, растворимые кислоты, соли, основания.
- Неэлектролиты — растворы не способные пропускать через себя электричество. Это нерастворимые в воде вещества, органические соединения. Например, азот, жидкий кислород.
Фарадей, изучая процесс распада ионов, задавался вопросом, можно ли «поймать» появляющиеся анионы и катионы. Как оказалось — вполне возможно. Для этого нужно просто создать окислительно-восстановительный процесс. В результате можно собрать на одной стороне катионы, а на другой анионы. Реакции диссоциации в электролите относятся к первичным процессам, а те, что протекают при восстановлении — вторичными.
Фактически это разделение и помогло Фарадею открыть два закона. Сегодня с помощью электролиза получают определённые марки металлов, обрабатывают поверхности. В промышленных масштабах его используют для очистки магния, натрия, алюминия. Электролиз находит также применение при фильтрации сточных вод.
Тест по теме
- /10
Вопрос 1 из 10Кто одновременно с Фарадеем открыл явление электромагнитной индукции?
Начать тест
Доска почёта
Чтобы попасть сюда — пройдите тест.
- Андрей Краков
8/10
- Дмитрий Конопинский
10/10
- Сергей Луценко
7/10
- Ирина Филимонова
9/10
Суть процесса электролиза
Электролизом называются процессы окислительно-восстановительных реакций, протекающие под принудительным воздействием электрического тока. Для его выполнения используется специальная емкость с электролитическим раствором, куда погружаются металлические штыри, соединенные с наружным источником питания.
Электрод, соединенный с полюсом отрицательного значения источника тока, считается катодом. Именно в данном месте частицы электролита восстанавливаются. Другой электрод подключается к плюсовому полюсу и носит название анода. На этом участке вещество электрода или частицы электролита окисляются. Химические реакции на этом участке происходят по-разному, в зависимости от материала анода и состава электролитического раствора. Поэтому, как утверждает химия, электроды по отношению к электролиту могут быть инертными или растворимыми.
К категории инертных относятся аноды, изготовленные из материала, не окисляющегося во время электролиза. В качестве примера можно привести графитовые или платиновые электроды. Растворимыми являются практически все остальные виды металлических анодов, подверженных окислению в ходе электролитической реакции.
Электролитами чаще всего служат различные виды растворов или расплавов, внутри которых происходит хаотичное движение заряженных частиц – ионов. Когда на них воздействует электрический ток, они начинают двигаться в определенном направлении: катионы – к катоду, анионы – к аноду. Попадая на электроды, они теряют свои заряды и оседают на них.
Индуктивность
Проходя по контуру, электрический ток способствует образование вокруг него совокупности магнитных силовых линий. Согласно формуле Ф = L×I, создаваемый магнитом поток Ф пропорционально зависит от силы тока I.
Таким образом, под индуктивностью L понимают коэффициент соотношения магнитного потока Ф и силы тока I, протекающего по контуру. Рассчитывают данную величину по следующей формуле:
L=Ф/I.
Единицей измерения этой физической величины является Генри (Гн). 1 Гн – это индуктивность, образующаяся в замкнутом контуре, в котором сила тока изменяется на 1 Ампер, а величина напряжения в нем составляет 1 Вольт.
Что мы узнали?
Фарадей, проводя реакцию электролиза разных веществ, вывел два закона. Согласно первому закону, масса вещества, осевшего на электрод, прямо пропорциональная количеству электричества, пропущенного через электролит: m = kq. Второй закон отражает взаимосвязь электрохимического эквивалента и эквивалентной массы вещества: k = (1/F) μeq. Электрохимический эквивалент – количество выделившегося вещества при прохождении единицы электричества. Эквивалентная масса – количество вещества, реагирующее с 1 молем водорода.
Способы определения ВТ при использовании импульсного тока
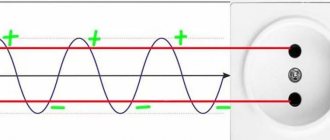
Если же через границу раздела фаз протекает импульсный ток, то при определении ВТ возникают большие трудности. Единой методики или прибора для определения ВТ при импульсном электролизе не существует. Сложность определения ВТ в условиях импульсного электролиза обусловлена тем, что проходящий через систему ток расходуется не только на электрохимическую реакцию, но и на заряжение двойного электрического слоя. Электрический ток, проходящий через границу раздела и вызывающий электрохимическое превращение, называется часто фарадеевским током. Ток заряжения расходуется на заряжение двойного электрического слоя, реорганизацию растворителя, самого реагента, т.е. на все на то, что создает условия для протекания электрохимической реакции, поэтому выражение для общего тока, проходящего через электрохимическую систему, будет выглядеть следующим образом:
I = Iз + Iф, где Iз – ток заряжения, Iф – фарадеевский ток.
Если не требуется определения абсолютных значений ВТ, то в качестве критерия оценки эффективности импульсного электролиза можно использовать отношения количества электричества, затраченного на растворение осадка к количеству электричества, затраченного на его формирование.