Свинцово кислотный аккумулятор – источник тока, питающий стартер при запуске двигателя. АКБ является основным источником энергии. Среди преимуществ данного типа аккумуляторных батарей – увеличенный срок службы, составляющий более 500 циклов, высокая удельная мощность, стоимость. Помимо транспортных средств, свинцовые аккумуляторы встречаются в резервных и аварийных источниках энергии стационарного и мобильного типа.
Принцип работы свинцово-кислотного аккумулятора заключается в преобразовании химической и электрической энергий.
Принцип работы
Основа принципа работы герметичного кислотного аккумулятора основана на электрохимической реакции диоксида свинца и свинца, которая происходит в водной суспензии серной кислоты. Во время заряда электроэнергия преобразуется в химическую. Когда АКБ питает внешний источник, химэнергия обратно преобразуется в электрическую, питая бортовую сеть автомобиля, стартер.
На скорость реакции, ёмкость воздействует окружающая температура. Если она увеличивается, предельная мощность увеличивается. Одновременно, возрастает риск деградации элементов, растёт склонность к корродированию.
Принцип действия
Принцип работы свинцово кислотного аккумулятора следующий:
- Реагент отрицательной решетки постепенно распадается под действием электролита, образуя ионы свинца. В результате этого распада появляются свободные электроны, которые затем попадают на положительную решетку электрода (через внешнюю цепь);
- Ионы свинца взаимодействуют с электролитом, образуя сульфат свинца. Из-за низкой растворимости он оседает на отрицательной решетке.
- В результате обычный свинец на отрицательной пластине превращается в сернокислый.
- Положительный электрод меньше взаимодействует с электролитом, чем отрицательный. Его основная составляющая – Pb02 реагирует с водой и делится на положительные и отрицательные ионы.
- Положительные передают на пластину соответствующий потенциал, где происходит их слияние с электронами. В ходе реакции восстановления образуется Pb2+, который далее реагирует с электролитом.
- Образовавшийся в результате сернокислый свинец скапливается на положительной решетке, образуя в последствии на ее поверхности свинцовый сульфат.
Батарея получает электроэнергию следующим образом:
- Возле обеих пластин в электролите содержится некоторое количество воды (H+, OH–) и сульфата свинца (Pb2+, SO2/4)
- В процессе зарядки электроны движутся с внешнего источника питания от положительного контакта батареи к отрицательному.
- Поступившие электроны восстанавливают свинец отрицательной пластины.
- Оставшиеся после восстановления свинца ионы и содержащийся в электролите H+ соединяются в H2SO
- На плюсовой пластине приходящий ток выбивает 2 электрона у 2-х валентного свинца, окисляя его до 4-х валентного.
- В результате последующих взаимодействий Pb4+ объединяется с ионами кислорода, восстанавливая материал плюсовой решетки.
- Оставшиеся ионы, реагируя между собой, компенсируют плотность электролита.
Особенности устройства
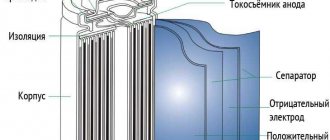
Аккумуляторная батарея состоит из следующих элементов:
Устройство свинцово-кислотного АКБ.
- Корпус. Блок из плотного композитного материала, как правило, пропилена, где заключены аккумуляторы.
- Электрод. Плоские решётки из свинца, куда запрессованы порошки диоксидов. Специальное покрытие увеличивает ёмкость батареи.
- Сепарат-конверт. Материал, защищающий аккумулятор от короткого замыкания. Он изолирует решётки, пластины противоположной полярности. Как правило, в производстве используется свинцово-кальциевый сплав, обладающий минимальным самозарядом.
- Выходные отверстия.
- Клеммы. Контактные блоки, через которые обеспечивается связь аккумулятора с генератором, стартером.
- Индикатор плотности и заряд. Небольшое окошко, позволяющее отследить текущий уровень заряда батареи.
Снятие аккумуляторных батарей
Перед тем, как приступить к снятию аккумуляторной батареи с автомобиля, необходимо ознакомиться с руководством по ремонту. Обратите внимание, что инструкция будет отличаться в зависимости от марки АКБ.
- Выньте ключ из замка зажигания.
- Снимите защитный колпачок с кожуха батареи и крышек полюсов (они иногда прикрепляются).
- Сначала отсоедините зажим аккумуляторного кабеля от отрицательной клеммы (если вы сначала отсоедините зажим аккумулятора от плюсовой клеммы, и она случайно соприкоснётся с кузовом, то это вызовет короткое замыкание.
- Затем отсоедините три остальных клеммы аккумуляторной батареи.
- Отсоедините соединительный кабель между аккумуляторами 1 и 2.
- Затем снимите оба крепления.
- Извлеките обе батареи из отсека.
Установка аккумуляторной батареи
Перед тем, как приступить к установке, необходимо ознакомиться с руководством по ремонту. Для каждой марки существует своя инструкция.
- Установите новые аккумуляторы.
- Очистите клеммы и зажимы.
- Установите соединительный кабель с зажимами на отрицательную клемму аккумулятора 2 (задний аккумулятор) и положительную клемму аккумулятора 1 (передний аккумулятор). Обратите особое внимание на клеммы, поскольку вывод «плюс» имеет больший диаметр, чем вывод «минус». Обе клеммы часто сужаются в верхней части.
- Установите зажим для положительной клеммы 2.
- Затем установите зажим для отрицательной клеммы 1.
- Смажьте клеммы и зажимы аккумулятора консистентной смазкой для предотвращения коррозии.
- Наденьте защитные колпачки на крышки полюсов (если они есть).
- Наденьте защитный чехол на корпус аккумуляторной батареи.
- Вставьте ключ в замок зажигания.
Разновидности
АКБ свинцово-кислотного типа делятся по типу электролита и по назначению. Во втором случае жидкость может быть абсорбируемой, жидкой, гелеобразной. Большинство моделей бюджетного, среднего сегмента имеют жидкую среду из раствора серной кислоты.
У более дорогих моделей электролит удерживается в специальном микропористом материале. Такие аккумуляторы имеют повышенную эффективную массу, как правило, устанавливаются в трансопртном средстве с системой рекуперативного торможения или стоп-старт.
По назначению автоаккумуляторы бывают:
- Тяговые. Когда требуется обеспечить устройство постоянной энергией. Как правило, такими батареями комплектуются тягачи, электрокары, погрузчики.
- Стартерные. Используются для запуска двигателя, когда требуется краткосрочная пиковая мощность.
Подробная классификация свинцово-кислотных АКБ.
Где применяются?
Решения позволяют работать с большими пиковыми мощностными нагрузками. Поэтому сфера использования батарей очень обширна. Установка возможна:
- На всех стартерных и ряде тяговых двигателей автомобилей.
- На мототехнике: мопедах, мотоциклах, квадроциклах, скутерах.
- На лодочных моторах.
- На авиационной технике.
- В качестве стартерных чаще используют решения с жидким электролитом, в качестве буферных, а также на сложной технике, включая авиационную, используют, преимущественно решения абсорбированным на сепараторе (по AGM -технологии).
Характеристики
При выборе аккумулятора автолюбители смотрят на параметры:
- Номинальная ёмкость. Параметр в А-ч, определяющий количество электричества, которое может передать модель.
- Стартерный ток. Способность автомобильной аккумуляторной батареи эффективно отдавать ток при заданной температуре. Как правило, показатель определяется при температуре -18°C, при длительности замеров – 30 секунд.
- Резервная ёмкость. Предельное время, в течение которого АКБ будет отдавать ток 25 Ампер до конечного напряжения 10,5 Вольт.
Циклическая и буферная работа АКБ
На некоторых батареях, на корпусе показывается максимальный ток зарядки и два напряжения, или фактически два диапазона напряжений.
Допустимое напряжение цикла использования применяется к циклической работе, то есть когда аккумулятор заряжается в течение нескольких часов, а затем разряжается в течение более длительного или более короткого времени. Примером может служить аккумулятор от электросамоката, работающий циклически.
С другой стороны, режим ожидания – это так называемая буферная работа, когда аккумулятор всегда под напряжением, готов к работе. Типичный пример – ИБП. Еще один пример – резервный источник питания для сигнализации. Тогда аккумулятор постоянно подключен к зарядному устройству – блоку питания, поэтому напряжение ниже, чем в циклическом режиме.
Как показано на фото, напряжение во время плавающего режима должно составлять 13,5 – 13,8 В, в циклическом режиме конечное напряжение заряда может составлять 14,4 – 15,0 В. Поскольку 12-вольтовая батарея имеет шесть ячеек, это дает 2,25 – 2,30 В / ячейку в буферном режиме и 2,4 – 2,5 В / ячейку в циклическом режиме.
Условия использования
Свинцово-кислотные батареи чувствительны к критическим температурам. По мере снижения внешних параметров окружающей среды, свойства АКБ ухудшаются, но в отличие от других типов аккумуляторов, потеря мощности не такая существенная, что и обуславливает их распространённость в автомобильной промышленности. Тесты показали, что при снижении внешней температуры на 1 градус ниже +20, ёмкость снижается на один процент. То есть при -20 АКБ деградирует примерно на 40%.
Зависимость емкости аккумулятора от температуры.
Такое поведение обусловлено снижением скорости химической реакции. Поэтому производители в северных широтах рекомендуют оставлять автомобиль в отапливаемом гараже либо подогревать АКБ специальным обогревателем, предусмотренным в ТС. Также существуют специальные модели с интегрированной системой подогрева.
В мороз следует контролировать плотность электролита. Если она будет ниже 1,10 г/см3, образуются кристаллы льда, что приводит к деформации свинцовых пластин, потере гарантии.
Защита от перезарядки батареи
Кислотные батареи имеют очень важное преимущество, заключающееся в том что напряжение отражает состояние заряда. Чтобы избежать перезарядки, просто не превышайте указанное в паспорте напряжение.
Зарядный ток обычно находится в диапазоне 0,1 C … 0,3 C (в некоторых случаях до 0,4 C), что численно составляет 10 … 30% емкости аккумулятора (C), выраженной в ампер-часах. Например, для аккумулятора емкостью C = 70 Ач ток 0,1 C равен 7 A, а 0,4 C – 28 А.
Обычно указывается максимальный зарядный ток данной батареи – например, максимальный зарядный ток обычных типовых автомобильных 12-вольтовых аккумуляторов составляет 3,6 А, то есть 0,3 С (30% от числового значения емкости).
Зарядка при 0,3 C в течение 3 часов 20 минут теоретически обеспечит аккумулятор номинальным зарядом (C). Но из-за недостаточной эффективности батареи полученный заряд должен быть больше, чем C.
Зарядка при постоянном токе в течение времени, возможно, будет приемлемой при низком зарядном токе, значительно ниже 0,1 C (10% емкости по количеству). Но это также может повлечь за собой газообразование. Проблема в том, что напряжение свинцовой батареи растет, и при значительном токе оно превысит допустимый уровень, что вызовет интенсивное выделение газов.
Теоретически можно использовать любой примитивный выпрямитель из лампочки и диодов, контролируя напряжение с помощью вольтметра и отключать заряд при повышении напряжения до предельного значения. На практике такой способ контроля не сработает. Человеческое участие должно быть исключено (чтоб не забыть отключить АКБ). Кроме того, многие производители сообщают, что AGM и гелевые аккумуляторы следует заряжать «плавным» постоянным током с минимально возможной пульсацией.
Поэтому для взаимодействия с гелевыми и AGM-аккумуляторами используются специальные зарядные устройства, которые по сути представляют собой стабилизаторы с определенным напряжением, обычно также содержащие схему ограничителя тока.
Самая популярная процедура зарядки CCCV
Схема зарядного устройства на 1 Ампер с ограничителем тока представлена на рисунке ниже. На начальном этапе зарядки аккумулятор заряжается постоянным током, определяемым номиналом резистора R3 (I ~ 0,7 В / R3). Когда падение напряжения на R3 приближается к 0,7 В, T1 начинает открываться, и напряжение понижается настолько чтобы поддерживать постоянный ток.
Схема зарядного устройства с ограничителем тока
В этой начальной фазе в зарядном устройстве срабатывает ограничитель тока и напряжение постепенно увеличивается. Когда напряжение достигает значения, определяемого R1 и R2 + P1, зарядное устройство начинает работать как обычный стабилизатор напряжения с блоком LM317 в простейшем включении. Напряжение больше не увеличивается, а это значит что когда аккумулятор почти полностью заряжен, ток автоматически начинает плавно уменьшаться, практически до нуля.
Зарядные характеристики авто АКБ
Процесс этой самой популярной процедуры зарядки, называемой CCCV (постоянный ток, постоянное напряжение), показан на рисунке. Предотвращение чрезмерного повышения напряжения эффективно предотвращает образование газов. Методом CCCV также заряжают литиевые батареи (Li-Ion, LiPo, LiFePO4), отличаются только допустимые токи и напряжения.
В основном обсуждался вопрос о максимальном токе зарядки. Стоит отметить, что в каталогах приведены характеристики такого заряда при относительно небольшом токе 0,1 С. Пример на рисунке. При таком токе время зарядки составляет 15 … 20 часов, что иногда будет недопустимо долгими.
Можно сократить время зарядки, увеличив ток до максимального значения по документации к АКБ. Тогда время зарядки будет в 1,5 … 2 раза меньше, чем это могло бы быть при делении номинальной емкости C на стандартный зарядный ток.
Преимущества и недостатки
Популярность таких типов АКБ объясняется следующими факторами:
- надёжность;
- низкая саморазрядка;
- простота в обслуживании (некоторые модели вовсе не требуют долива электролита, дополнительного сервиса);
- доступная цена, что объясняется низкой себестоимостью.
Помимо достоинств, свинцово-кислотные батареи не лишены негативных моментов:
- для длительного хранения АКБ должна иметь полный заряд;
- плохая переносимость глубокого разряда;
- ограниченное количество циклов зарядки-разрядки;
- компоненты, из которых производится аккумулятор, вредны для окружающей среды;
- батарею следует правильно заряжать. При нарушении уровня напряжения существует риск перегрева банок;
- нестабильная работа при экстремальных температурах. Если не соблюдать обозначения, указанные на информационном стикере, автомобиль будет плохо заводится зимой при критических температурах.
Срок службы
Качественная батарея, изготовленная с соблюдением технологий, прослужит в 2-3 раза дольше, чем дешевая продукция сомнительного бренда с гарантией 6 месяцев. Имеются ввиду одинаковые типы АКБ и такие же режимы нагрузок на них.
Батарея средней ценовой категории с гарантией 2 года при умеренных стартерных нагрузках пройдет около 100 тыс. км или прослужит 3-5 лет. Эксплуатация в более интенсивных режимах, например, в такси сократит срок службы минимум вдвое. Если к этому прибавить работу преимущественно в условиях низких температур, халатное отношение к обслуживанию, несколько циклов полного разряда, то даже качественная батарея вряд ли выдержит больше года.
Эксплуатация
Чтобы свинцово-кислотные аккумуляторы прослужили дольше заявленного гарантийного срока, следует соблюдать некоторые правила эксплуатации.
Работа
Если АКБ обслуживаемый (банки открываются для долива электролита), при движении по неровной поверхности происходит незначительное просачивание электролита из-под крышек н корпус. Для исключения глубокого саморазряда рекомендуется регулярно протирать корпус разведённым в воде хоз. мылом или раствором соды. Таким образом, нейтрализуется электролит.
Следует контролировать и уровень электролита, не допуская оголения пластин (в этом случае увеличивается саморазряд, батареи окисляются).
Хранение
Зависимость срока хранения аккумулятора от температуры окружающей среды.
Кислотные АКБ в снятом состоянии могут храниться исключительно с полным зарядом. Если температура в боксе ниже -20°C ежегодно следует ставить аккумулятор на подзарядку в течение 48 часов (напряжение 2,45 V). При комнатной температуре в месте хранения подзаряд достаточно осуществлять каждые 8 месяцев в течение 8-12 часов.
Поверхность АКБ следует содержать в чистоте. Это исключает саморазряда АКБ, что чревато потерей ёмкости, связанной с образованием сульфида повышенной плотности, который хуже вступает в реакцию.
Если автомобиль не используется зимой, следует подготовить аккумулятор, выполнив следующие действия:
- провести полную зарядку в соответствии с рекомендациями производителя;
- нанести на положительную клемму пластичную смазку, исключив абсорбирование влаги на поверхности;
- хранить АКБ при температуре в пределах 0 -10 °C, исключая промерзания жидкости внутри банок.
В случае необходимости поездки в морозы следует перенести аккумулятор в отапливаемое помещение, и в течение 7—9 часов (например, за ночь) он придёт в пригодное для пуска двигателя состояние.
Правила утилизации
Ни в коем случае не стоит самостоятельно разбирать АКБ, пытаясь достать свинец для вторичного использования в быту. Как и другие батареи, свинцово-кислотный аккумулятор необходимо сдать в специализированный сервис. Как правило, они действуют в местах покупки. В рамках промышленной утилизации может предоставляться скидка на покупку новой батареи.
Индикатор емкости
Стандартным способом проверки емкости АКБ принято считать контрольный разряд. Полностью заряженную АКБ разряжают постоянным током. Сила потребляемого тока должна быть кратной емкости батареи (оптимальным считается соотношение 1 к 20). Например, при номинальной емкости 60 Ah свинцово кислотный аккумулятор разряжают током 3 A в течение 20 часов.
Вышеописанный способ достаточно трудоемок и сложен, к тому же во время проведения замеров батареей нельзя пользоваться. Чтобы быстро протестировать свинцовый аккумулятор следует использовать специальные устройства, такие как «Нагрузочная вилка» или подобные им индикаторы емкости .
Вторичная переработка
Свинец, содержащийся в АКБ – токсичный тяжёлый металл, способный нанести серьёзный урон окружающей среде. Свинец и его соли, образованные в результате работы батареи, должны быть утилизированы в промышленных условиях.
Утилизация АКБ происходит на перерабатывающих предприятиях, имеющих все необходимое оборудование.
Правила утилизации
Закажите спецтехнику на нашем сайте: Аренда спецтехники в России
Средний срок эксплуатации свинцового аккумулятора для автомобиля составляет от двух до пяти лет или до 130-150 тысяч километров. Невыполнение правил, рассмотренных выше, приводит к быстрому выходу устройства из строя. Отработанные свинцовые аккумуляторы нельзя просто выбросить на мусорку. Здесь доступно несколько путей:
- Сдача в специализированные пункты приема.
- Обмен в магазине на новый АКБ с получением скидки.
- Передача частным лицам за определенную оплату. Но нужно учесть, что в таком случае высок риск получить меньше денег, а сами лица редко имеют лицензию на сбор опасных компонентов.
Свинцовые аккумуляторы для грузовиков требует особого внимания из-за работы в сложных условиях эксплуатации. Для продления срока службы необходимо следовать правилам обслуживания, контролировать состояние АКБ и своевременно выполнять подзарядку.
Как выбрать аккумулятор
Выбор моделей, представленных в магазинах, велик. Чтобы купить свинцово-кислотный АКБ, рекомендуется обращать внимание на следующие нюансы:
- Размер. При подборе аккумулятора важен размер, который должен соответствует нише в моторном отсеке.
- Полярность. Расположение клемм нового АКБ и старого должны совпадать.
- Бренд. Эксперты рекомендуют выбрать аккумулятор для автомобиля известного производителя, что гарантирует качество продукции в течение заявленного срока.
- Тип. Обслуживаемый или необслуживаемый. Во втором случае батарея не требует дополнительного ухода, но при глубоком переразряде её нельзя будет регенерировать.
- Заявленный ток. Чем выше параметр, тем ниже внутренне сопротивление, тем качественней модель.
Свинцово-кислотная батарея из-за потребительских характеристик – практически безальтернативный вариант для установки в автомобиле. При этом производители предлагают сотни вариантов, отличающихся по цене, техническим характеристикам, ориентированных на разных клиентов.
Cистематизируем знания, обретаем навыки: дистанционное обучение
Итак, вы познакомились с теорией, касающейся АКБ, классификацией, способами восстановления, зарядкой, но хотите изучить тему глубже, максимально систематизировать знания по этому вопросу, научиться на практике работать с батареей, протестировать свои знания? Отлично!
Вам поможет система онлайн-обучения механиков, электриков и диагностов ELECTUDE. Огромное преимущество онлайн -платформы состоит в том, что она максимально ориентирована на комплексный подход (основы физики + практикоориетированные материалы), и вы сможете получить не просто знания, но и конкретные умения, навыки, а система оценки знаний в виде тестов поможет реально оценить, над какими темами темами еще стоит поработать, в каком темпе двигаться дальше.
Далее мы приводим скриншоты и описания переведённых нами на русский язык модулей, которые непосредственно касаются рассматриваемой выше темы.
Изучайте, присматривайтесь к системе ELECTUDE и находите для себя новый источник не просто для получения знаний, а для пошагового развития практических навыков. Ведь кроме базовых модулей в системе есть специальный виртуальный тренажёр. Он и поможет «прокачаться» по полной. Система отлично подходит для обучения в дистанционном формате, самообучения.
Кислотные аккумуляторы; чтобы больше не было отвратительно читать то что люди о них пишут
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить. Начнем с названия. Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там. С химической точки зрения любые АКБ абсолютно одинаковы
. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:
Тут мы видим, что в форсированном режиме напряжение заряда
может быть аж 15В.
Все разъяснит кривая напряжения на АКБ:
Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
1 Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
2 Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
3 Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды. Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2H2O = 2H2 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно
происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции. Про них бытуют следующие мифы:
1.
Водород крайне взрывоопасен! Перезарядишь аккумулятор и как минимум лишишься комнаты где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты. Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества H2 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства. Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2.
При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
3.
При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут
увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги. Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду. Процедура доливания воды — необходимая часть процесса обслуживания
любой АКБ. Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т.н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + SiO2
+ H2O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
1. Малогабаритные и крупногабаритные АКБ идентичны по устройству.
2. Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
3. Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
4. Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
5. Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
6. Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
Выводы
В вопросе, какой аккумулятор лучше, свинцово кислотный или литиевый, нет единого мнения. Несмотря на стремительное развитие литиевых технологий, АКБ не сдают позиций и все еще используются при оснащении складской техники, гольфкаров, ИБП и других устройств. Но в силу объективных преимуществ литиевые АКБ все чаще становятся приоритетными.
При выборе оптимального источника питания сегодня лидируют литий-железо-фосфатные батареи. Они имеют стабильную химическую структуру, широкий диапазон рабочих температур и большой циклический ресурс, быстро заряжаются, не боятся глубокого разряда и жестких условий эксплуатации. Такие АКБ часто используются в качестве тяговых батарей для электротранспорта, лодочных моторов, клининговой и складской техники.
В предыдущей статье нашего блога приведены рекомендации по эксплуатации литий-титанатных аккумуляторов.